Infórmese sobre los nuevos tratamientos para el Parkinson y cómo conseguirlos en Chile antes de que se aprueben a nivel local.


Infórmese sobre los nuevos tratamientos para el Parkinson y cómo conseguirlos en Chile antes de que se aprueben a nivel local.


¿Cómo puede acceder a los últimos tratamientos contra el cáncer de pulmón antes de que estén disponibles en Polonia?

El primer medicamento para la enfermedad del hígado graso con fibrosis aún no está aprobado en Polonia, pero puede conseguirlo. He aquí cómo.


¿Cuáles son las inmunoterapias más novedosas contra el cáncer de cuello de útero y cómo conseguirlas de inmediato en Polonia?


¿Cuándo estará disponible en Suiza el último medicamento contra el Alzheimer (y cómo conseguirlo antes)?


¿Está disponible el nuevo medicamento contra el Alzheimer para los pacientes suizos, y cómo se puede conseguir?


Ya está disponible un nuevo medicamento eficaz y seguro para reducir los triglicéridos en pacientes con SFC. Pero, ¿cuándo estará disponible para usted?

¿Cuándo estará disponible en Europa y el Reino Unido el primer medicamento aprobado para el hígado graso con fibrosis?


¿Cuándo estará disponible el nuevo medicamento contra la EPOC para los pacientes de Europa y el Reino Unido (y cómo no esperar)?

¿Cuándo estará disponible para los pacientes europeos la primera terapia dirigida para el cáncer gástrico y de la EGJ CLDN 18.2 positivo?

¿Cuándo estará disponible fuera de EE.UU. la primera terapia dirigida para la leucemia aguda con translocación KMT2A?
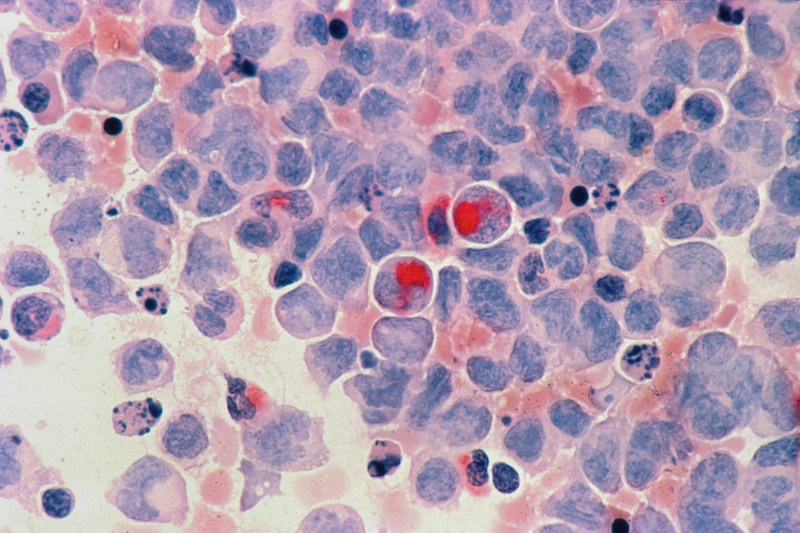

¿Cuándo estará disponible el primer medicamento contra la CNF para los pacientes de Europa, el Reino Unido y otros países (y cómo no esperar)?


¿Cuándo se aprobará la primera terapia dirigida contra el CMB HER2? Todo sobre los plazos y sus opciones mientras tanto.


Todas las opciones seguras y legales para acceder a Leqembi mientras espera su aprobación en la UE.

A continuación se ofrece una descripción general de cada medicamento para ayudarle a usted y a su médico a tomar una decisión sobre el tratamiento de la fibrosis quística: 
La terapia contra el Parkinson de Kyowa Hakko Kirin, Nourianz istradefylline), obtiene la aprobación de la FDA como complemento de la levodopa.

Radicutedaravone), que ha demostrado ralentizar la progresión de la ELA, ya está aprobado para pacientes en China.

Orkambi y Symkevi han sido rechazados por el Consorcio de Medicamentos de Escocia (SMC) debido a su conclusión de que los costes superan a los beneficios.

Vitrakvi larotrectinib) recomendado por el CHMP para su aprobación en la UE.

Nuevo medicamento contra el cáncer de piel aprobado ahora en la UE para adultos con carcinoma cutáneo de células escamosas metastásico o localmente avanzado.

Vyndaqel tafamidis) ya está aprobado en EE.UU. después de que un estudio demostrara un aumento de la tasa de supervivencia y una reducción del tiempo de hospitalización por problemas relacionados con el corazón.

La aprobación de la siguiente fase de ensayos clínicos sitúa a los pacientes de ELA un paso más cerca de acceder a un nuevo tratamiento que ralentiza la progresión de la enfermedad.
Basándose en los prometedores resultados de los ensayos clínicos de fase III, Health Canada ha decidido ampliar el uso de Kalydeco (ivacaftor) para incluir a los niños de 1 a 2 años.

Un reciente ensayo clínico indica que Symdeko (tezacaftor/ivacaftor) puede aflojar de forma segura y eficaz la mucosidad espesa y pegajosa en niños de 6 a 11 años.

Un ensayo de fase III demuestra que Copiktra duvelisib) puede ser una opción para los pacientes con leucemia linfocítica crónica y linfoma linfocítico pequeño en recaída o resistentes al tratamiento.

Onpattro (patisiran) es el primer tratamiento de su clase que frena la progresión de la amiloidosis hereditaria por transtiretina (hATTR).

Un nuevo medicamento muestra mejoras estadísticamente significativas para los pacientes con cáncer de próstata.

Australia reembolsa los medicamentos para la fibrosis quística.

La Comisión Europea ha aprobado Alunbrig brigatinib) para el tratamiento de un tipo específico de cáncer de pulmón.
