Briumvi vs Ocrevus vs Kesimpta: Opciones de tratamiento de la EM
Última actualización: 15 de enero de 2024

Puede acceder legalmente a nuevos medicamentos, aunque no estén aprobados en su país.
Más informaciónSi está navegando por el panorama de los tratamientos de la esclerosis múltiple (EM), es posible que Briumvi, Ocrevus y Kesimpta estén en su radar. Este resumen le ayudará a comprender las principales similitudes y diferencias entre estos tres importantes tratamientos de la EM.
Abarca desde sus usos, mecanismos de acción, métodos de administración, eficacia, efectos secundarios, hasta costes y autorizaciones.
Brumvi vs Ocrevus vs Kesimpta: ¿Para qué se utilizan?
Similitudes
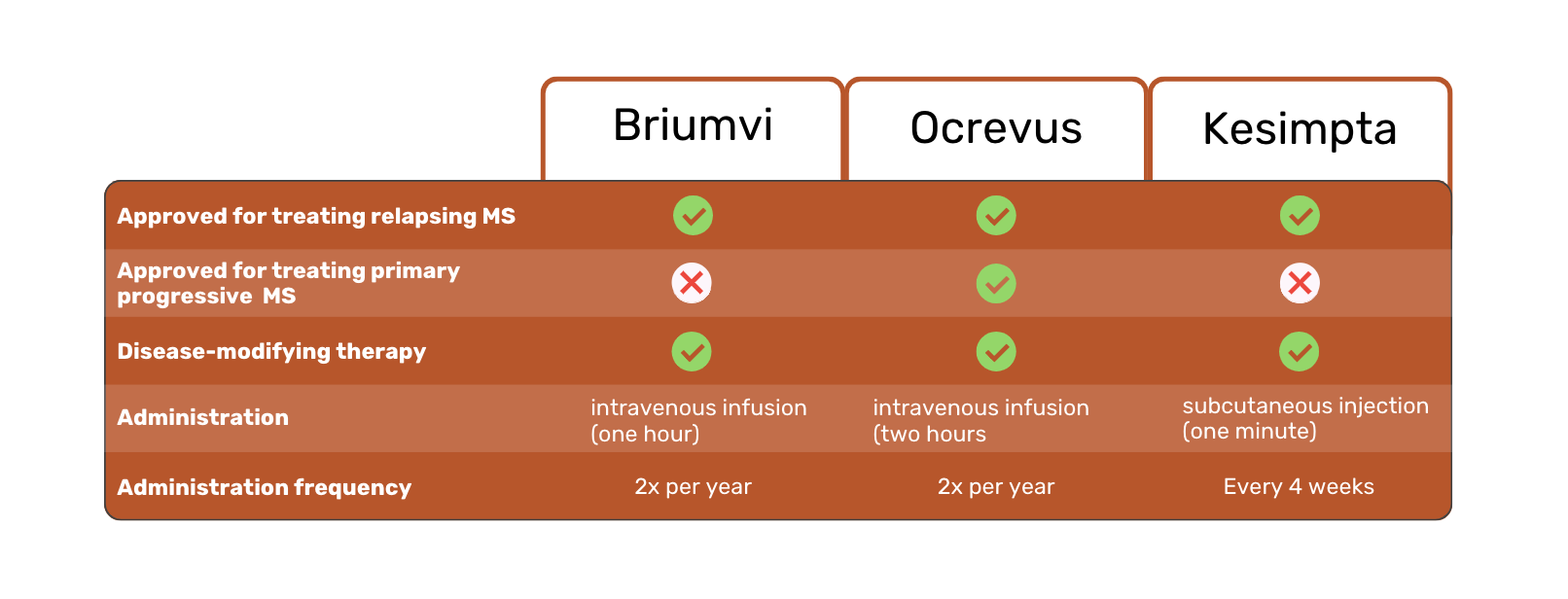
Las tres terapias se prescriben para el tratamiento de la Esclerosis Múltiple (EM). Más concretamente, la EM recurrente (EMR), que incluye el síndrome clínicamente aislado, la EM recurrente-remitente y la EM secundaria progresiva activa 1,2,3.
Diferencias
Ocrevus es el único medicamento de los tres aprobado por la FDA para el tratamiento de pacientes con EM primaria progresiva (EMPP) 1.
Briumvi vs Ocrevus vs Kesimpta: ¿Cómo funcionan?
Briumvi, Ocrevus y Kesimpta son terapias modificadoras de la enfermedad. En otras palabras, su objetivo es ralentizar la progresión de la EM y abordar su causa subyacente, en lugar de centrarse únicamente en sus síntomas.
Los tres medicamentos son anticuerpos monoclonales anti-CD20 y, en general, su mecanismo de acción es bastante similar. Aún no se sabe muy bien cómo actúan, pero los tres medicamentos se dirigen a células B específicas que expresan la proteína CD20. Se cree que estas células están implicadas en la progresión de la EM.
Al atacar estas células B, Briumvi, Kesimpta y Ocrevus pretenden reducir las tasas de recaída de la EM, ralentizar la progresión de la enfermedad y disminuir las lesiones cerebrales activas en los pacientes con EM 4.
¿Cómo se administran Briumvi, Ocrevus y Kesimpta ?
Existen algunas diferencias notables en la administración de las tres terapias.
Briumvi y Ocrevus están disponibles como infusiones intravenosas. En cambio, Kesimpta se inyecta en la piel. Esta es una diferencia importante, ya que permite a los pacientes de Kesimpta autoinyectarse en casa, en lugar de recibir una infusión en un hospital o clínica.
Otra diferencia entre los tres tratamientos de la EM es la frecuencia y duración de la administración. Briumvi requiere infusiones de una hora dos veces al año. En comparación, Ocrevus requiere dos infusiones de dos horas al año. Las inyecciones de Kesimpta son necesarias cada cuatro semanas.

¿Cuál es la eficacia de Briumvi, Ocrevus y Kesimpta?
En términos de eficacia, los tres medicamentos han mostrado resultados similares en la reducción de las recaídas y la ralentización de la progresión de la EMR. A continuación se exponen algunos aspectos destacados de los resultados de sus ensayos clínicos.
Ocrevus resultados de ensayos clínicos
-
Resultados en pacientes con EMR
En 2 ensayos clínicos de más de 2 años de duración, Ocrevus se comparó con otro tratamiento aprobado para la EM, Rebif.
Los resultados de los estudios mostraron una reducción del 46% de las recaídas en los pacientes de Ocrevus , en comparación con los de Rebif. El 83% de los que tomaron Ocrevus no experimentaron recaídas, frente al 71% de los que tomaron Rebif 4.
A lo largo de los 2 años que duraron los estudios, las personas que tomaban Ocrevus tenían un 40% menos de probabilidades de sufrir una progresión de la discapacidad que las que tomaban Rebif. En cuanto a las lesiones T1 Gd+, los pacientes de Ocrevus experimentaron un 94% menos de lesiones que los de Rebif. La reducción de las lesiones se considera un elemento importante para ralentizar la progresión de la EM 4.
-
Resultados en pacientes con EMPP
Para evaluar su seguridad y eficacia en pacientes con EMPP, se probó Ocrevus frente a un placebo.
Los resultados del estudio clínico mostraron que el 32,9% de los pacientes que tomaron Ocrevus experimentaron una progresión de la discapacidad, frente al 39,3% de los que tomaron placebo.
Los pacientes tratados con placebo experimentaron un aumento del 7% en el volumen de la lesión T2, mientras que los pacientes tratados conOcrevus experimentaron una reducción del 3% en el volumen de la lesión T2.
Resultados de los ensayos clínicos con Briumvi
La eficacia y seguridad de Briumvi se probaron en 2 ensayos clínicos frente a otro tratamiento de la EM: la teriflunomida.
Los resultados de los ensayos clínicos mostraron que los pacientes que tomaron Briumvi experimentaron un 49% (Ensayo 1) y un 59% (Ensayo 2) menos de rec aídas que los que tomaron teriflunomida. De las personas que tomaron Briumvi, el 86% (Ensayo 1) y el 87% (Ensayo 2) no tuvieron recaídas, en comparación con el 74% (Estudio 1) y el 72% (Estudio 2) de los pacientes de teriflunomida.
Los pacientes con Briumvi presentaron un 97% (Ensayos 1 y 2) menos de lesiones T1 Gd+ que los pacientes con teriflunomida.
Kesimpta resultados de ensayos clínicos
De forma similar a Briumvi, Kesimpta se probó frente a teriflunomida en 2 ensayos clínicos.
Los resultados mostraron un 51% (ensayo 1) y un 58% (ensayo 2) menos de recaídas en los pacientes de Kesimpta en comparación con los de teriflunomida.
La progresión de la discapacidad tras el inicio de los síntomas de discapacidad fue un 34% (3 meses después del inicio de los síntomas) y un 33% (6 meses después del inicio de los síntomas) menos probable para los pacientes de Kesimpta que para los pacientes de teriflunomida.
Kesimpta presentaron un 98% (Ensayo 1) y un 94% ( Ensayo 2) menos de lesiones T1 Gd+ en comparación con los pacientes tratados con teriflunomida. Los pacientes tratados con Kesimpta también presentaron un 82% (Ensayo 1) y un 85% (Ensayo 2) menos de lesiones T2.


Briumvi vs Ocrevus vs Kesimpta: Seguridad y efectos secundarios
Según su información de prescripción, los efectos secundarios más frecuentes asociados a los tratamientos con Briumvi, Ocrevus y Kesimpta son en su mayoría similares. A continuación se ofrece una visión general, con algunos matices.
Efectos secundarios de Briumvi
- Reacciones a la infusión, incluyendo fiebre, escalofríos, dolor de cabeza, síntomas similares a los de la gripe 5.
- Infecciones. La tasa global de infecciones fue del 56%, con un 5% consideradas graves. Las infecciones más frecuentes fueron las del tracto respiratorio superior y las del tracto urinario 5.
Ocrevus efectos secundarios
- Reacciones a la infusión, incluyendo picor en la piel, erupciones, dificultad para respirar, hinchazón y dolor de garganta, hipotensión, fiebre, cansancio 6.
- Infecciones. La tasa global de infecciones fue del 58%. Las infecciones más frecuentes fueron las del tracto respiratorio superior e inferior, así como las cutáneas y las relacionadas con el herpes 6.
Kesimpta efectos secundarios
- Reacciones relacionadas con la inyección, como hinchazón, picor y dolor 7.
- Infecciones. La tasa global de infecciones fue del 51,26%-52,7%, con un 1,8%-2,5% consideradas graves. Las infecciones más frecuentes fueron las del tracto respiratorio superior y las del tracto urinario 7.
- Dolor de cabeza.
¿Briumvi, Kesimpta o Ocrevus provocan leucoencefalopatía multifocal progresiva (LMP)?
La LMP es una infección vírica rara del cerebro, que suele observarse en personas inmunodeprimidas. Se han notificado algunos casos de LMP tras el tratamiento con Ocrevus 6.
Aunque actualmente no se han registrado casos de LMP tras un tratamiento con Briumvi o Kesimpta , es importante tener en cuenta que la LMP puede aparecer tras el tratamiento con cualquiera de estas terapias.
Briumvi vs Ocrevus vs Kesimpta: Comparación de precios
Cuando se trata de medicamentos que aún no están ampliamente disponibles, los costes tienden a variar en función de su ubicación, los proveedores o la cobertura del seguro.
A continuación se ofrece una aproximación de los costes anuales del tratamiento con Briumvi, Ocrevus, y Kesimpta, suponiendo que no haya cobertura de seguro.
¿Cuánto cuesta Briumvi sin seguro?
Para los pacientes de EE.UU., donde Briumvi está aprobado y disponible en el mercado, el coste anual del tratamiento se estima en 59.000 USD. Esta suma cubre 2 infusiones de 450 mg (6 viales en total). A este precio, Briumvi es el tratamiento de la EM más asequible en EE.UU. en este momento 13.
Sin embargo, la situación es diferente para los pacientes de la UE y otras regiones fuera de los EE.UU.. Aunque Brumvi está aprobado en la UE, aún no está disponible comercialmente allí, lo que supone mayores costes de abastecimiento. En cuanto se fije el precio de Briumvi en la UE y el tratamiento esté disponible localmente, es probable que también baje el precio para los pacientes no estadounidenses. Hemos observado una tendencia similar con Kesimpta y Ocrevus, que llevan varios años en el mercado de la UE.
Mientras tanto, una dosis única de 150 mg (6 ml) de Briumvi fuera de EE.UU. cuesta unos 15.130 EUR. Esto se traduce en un coste de tratamiento anual de unos 90.780 EUR (6 viales).
¿Cuánto cuesta Kesimpta sin seguro?
Una dosis única de 20 mg (0,4 ml) de Kesimpta cuesta unos 1.700 euros.
El tratamiento suele comenzar con una dosis inicial de 20 mg (0,4 ml), que se repite una semana y dos semanas después. Las inyecciones posteriores se realizan una vez al mes.
Esto significa que sus costes anuales de tratamiento serán de unos 25.500 EUR el primer año, y bajarán a unos 20.400 EUR después.
¿Cuánto cuesta Ocrevus sin seguro?
Una dosis única de Ocrevus (300 mg/mL) cuesta alrededor de 8,016 EUR.
El tratamiento suele comenzar con una dosis inicial de 300 mg, que se repite dos semanas después. Las infusiones posteriores se realizan una vez cada 6 meses, a una dosis recomendada de 600 mg.
Esto supone unos 48.096 EUR de costes de tratamiento el primer año, que se reducen a 32.064 EUR después.


¿Dónde están homologados Briumvi, Ocrevus y Kesimpta ?
Briumvi y Kesimpta sólo están aprobados actualmente en EE.UU. y la UE 8, 9, 10, 11. Ocrevus está aprobado actualmente en más de 98 países, incluidos EE.UU., la UE, Canadá, Australia y Nueva Zelanda 12.
¿Briumvi, Ocrevus o Kesimpta no están (aún) aprobados o disponibles en su país? Si usted y su médico opinan que estos tratamientos podrían beneficiarle, póngase en contacto con nuestro equipo de expertos en acceso médico. Podemos darle un presupuesto personalizado para conseguirle el medicamento.
Referencias:
- OCREVUS® (ocrelizumab) | Tratamiento de la esclerosis múltiple (EM). Ocrevus, Consultado el 22 de agosto de 2023.
- Tratamiento de la EM recidivante I KESIMPTA® (ofatumumab). Kesimpta, Consultado el 22 de agosto de 2023.
- BRIUMVI ® (ublituximab-xiiy). Briumvi, consultado el 22 de agosto de 2023.
- OCREVUS® (ocrelizumab) Resultados para la EMR (EM recurrente). Ocrevus, Consultado el 22 de agosto de 2023.
- ID de referencia: 5101565. TG Therapeutics, consultado el 22 de agosto de 2023.
- PUNTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN. Genentech, consultado el 22 de agosto de 2023.
- PUNTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN. Novartis, consultado el 22 de agosto de 2023.
- Briumvi | Agencia Europea de Medicamentos. Agencia Europea de Medicamentos, 13 de julio de 2023.
- Aprobación de BRIUMVI™ (ublituximab-xiiy) | TG Therapeutics, Inc. TG Therapeutics, 28 de diciembre de 2022.
- La FDA aprueba Kesimpta® (Ofatumumab), la primera terapia autoadministrada con células B para las formas recidivantes de la EM | MSAA. Asociación Americana de Esclerosis Múltiple, 25 de agosto de 2020.
- Kesimpta | AgenciaEuropea de Medicamentos. Agencia Europea de Medicamentos, 29 de enero de 2021.
- Ocrevus. Roche, consultado el 22 de agosto de 2023.
- La FDA aprueba Briumvi (ublituximab-xiiy) para la EM recurrente. Sociedad Nacional de EM, 28 de diciembre de 2022.