Adakveo frente a Oxbryta: Conozca las alternativas crizanlizumab
Última actualización: 15 de enero de 2024
Puede acceder legalmente a nuevos medicamentos, aunque no estén aprobados en su país.
Más información
Tras la revocación de la autorización de Adakveo crizanlizumab) en la UE, muchos pacientes y médicos necesitan encontrar una alternativa a Adakveo .
Si ha respondido bien a su tratamiento, aún puede acceder a Adakveo aunque ya no esté aprobado en la UE. Sin embargo, si su médico prefiere cambiar el curso de su tratamiento, es bueno entender lo que esto significa para usted como paciente.
En este artículo examinaremos una de las posibles alternativas a Adakveo que su médico puede querer discutir: Oxbryta voxelotor). Aquí encontrará un breve resumen de las similitudes y diferencias entre Adakveo y Oxbryta.
Adakveo vs Oxbryta: ¿Para qué se utilizan?
Tanto Adakveo como Oxbryta son medicamentos de venta con receta indicados para el tratamiento de la anemia falciforme 1,2. Sin embargo, cada uno de ellos se dirige a un aspecto diferente de la enfermedad.
Adakveo tiene por objeto reducir la frecuencia de las crisis vaso oclusivas dolorosas, mientras que Oxbryta se utiliza para tratar la anemia hemolítica en pacientes con drepanocitosis 1,2.
¿Para qué edad está autorizado Oxbryta en la UE?
A diferencia de Adakveo, que sólo puede utilizarse en pacientes mayores de 16 años, Oxbryta también está indicado para pacientes pediátricos.
En EE.UU., Oxbryta puede prescribirse a partir de los 4 años, mientras que en la UE, el uso pediátrico sólo está aprobado a partir de los 12 años 1,2.
Crizanlizumab frente a Voxelotor: ¿Cómo funcionan?
Aunque ambos medicamentos pretenden reducir las complicaciones de la anemia falciforme, se dirigen a aspectos diferentes de la enfermedad.
Adakveo y la reducción de las crisis dolorosas
Adakveo pretende reducir la frecuencia de las crisis dolorosas, que se producen cuando células sanguíneas malformadas se atascan en los vasos sanguíneos.
El principio activo del medicamento, crizanlizumab, es un tipo específico de proteína conocida como anticuerpo monoclonal. Esta proteína está formulada para unirse a la P-selectina, una sustancia que se encuentra en la capa externa de las células que recubren los vasos sanguíneos.
La P-selectina ayuda a las células a adherirse a los vasos sanguíneos y está implicada en la obstrucción de los vasos durante los episodios dolorosos de la anemia falciforme. Al conectarse a la P-selectina e inhibir su función, Adakveo pretende prevenir estos episodios dolorosos 3.
Oxbryta y la prevención de la anemia
Oxbryta, por su parte, pretende prevenir la anemia asociada a la anemia falciforme.
El principio activo de Oxbryta, voxelotor, mejora la capacidad de la hemoglobina para retener oxígeno e impide que forme cadenas rígidas dentro de los vasos sanguíneos. Esto ayuda a los glóbulos rojos a mantener su forma y flexibilidad normales. También reduce el ritmo de su destrucción prematura y prolonga su vida 4.
¿Cuál es la eficacia de Adakveo y Oxbryta?
La eficacia de Adakveo crizanlizumab) y Oxbryta voxelotor) se ha estudiado en ensayos clínicos.
-
Resultados de los ensayos clínicos Adakveo
La aprobación de Adakveo por la FDA, así como su autorización inicial de comercialización en la UE, se basaron en los resultados del estudio clínico SUSTAIN. El estudio comparó Adakveo (con o sin hidoxiurea) frente a placebo.
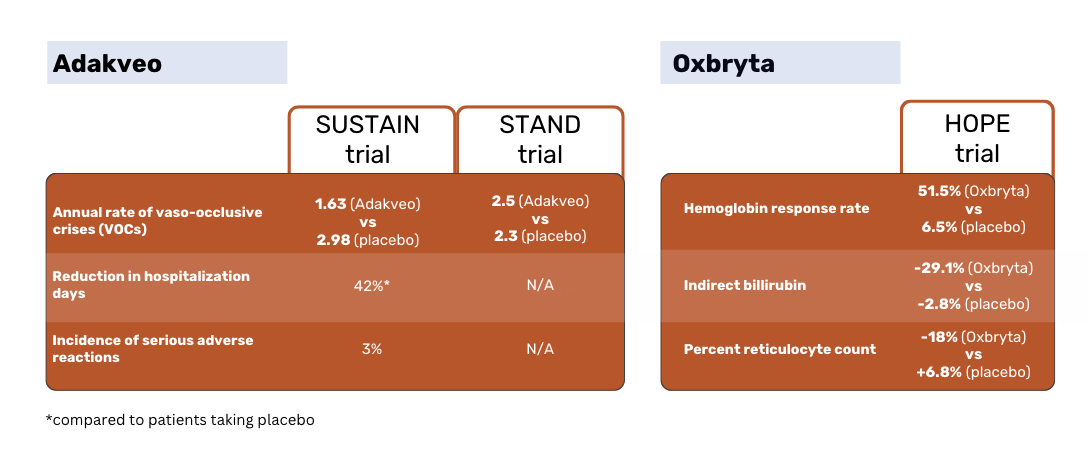
Según los resultados del estudio SUSTAIN, los pacientes tratados con Adakveo presentaron una tasa media anual de crisis vaso-oclusivas (CVO) inferior y estadísticamente significativa: 1,63 frente a 2,98 en el caso de los pacientes tratados con placebo. El 36% de los pacientes tratados con Adakveo no sufrió ninguna crisis vaso-oclusiva durante las 52 semanas del ensayo, frente al 17% de los tratados con placebo 1.
¿Cuáles fueron los resultados del ensayo STAND Adakveo ?
El estudio STAND global de fase 3, que volvió a comparar Adakveo frente a placebo, no logró demostrar una diferencia estadísticamente significativa en la tasa de COV entre los grupos de pacientes. Los pacientes tratados con Adakveo tuvieron una media de 2,5 crisis dolorosas al año de tratamiento, lo que no difiere significativamente de las 2,3 crisis de media notificadas en el grupo placebo 3.
Los resultados poco convincentes del juicio STAND se convirtieron en la base de la revocación deAdakveo en la UE.
-
Resultados de los ensayos clínicos Oxbryta
En el ensayo HOPE, Oxbryta se comparó con placebo. La eficacia se basó en las tasas de respuesta de la hemoglobina (Hb), definidas como un aumento de la Hb de >1 g/dL desde el inicio hasta la semana 24.
La tasa de respuesta de los pacientes tratados con Oxbryta fue del 51,1%, frente al 6,5% de los tratados con placebo. La bilirrubina indirecta disminuyó un 29,1% en los pacientes tratados Oxbryta , frente a una disminución del 2,8% en los pacientes tratados con placebo. El porcentaje de reticulocitos disminuyó un 18% en los pacientes tratados Oxbryta y aumentó un 6,8& en los tratados con placebo 2.
Como muestran los datos compartidos, no es posible hacer una comparación directa entre los dos medicamentos, ya que en sus ensayos clínicos se utilizaron criterios de eficacia diferentes. Dado que ambos tratamientos abordan la anemia falciforme de forma diferente, es probable que Oxbryta no sustituya directamente a Adakveo, sino que forme parte de un nuevo plan de tratamiento que tu médico elaborará para ti.

Adakveo frente a Oxbryta: Seguridad y efectos secundarios
Según su información de prescripción, estos son los efectos secundarios más comunes de Adakveo y Oxbryta:
Efectos secundarios Adakveo
- Náuseas
- Dolor articular
- Dolor de espalda
- Dolor de estómago
- Fiebre1.
Durante el ensayo SUSTAIN, el 3% de los pacientes experimentaron reacciones relacionadas con la infusión, caracterizadas por síntomas como dolor de cabeza, escalofríos, vómitos, diarrea, dificultad respiratoria o sibilancias 1.
Efectos secundarios Oxbryta
- Dolor de cabeza
- Diarrea
- Dolor de estómago
- Náuseas
- Erupción
- Fiebre 2.
Menos del 1% de los pacientes de ensayos clínicos experimentaron reacciones de hipersensibilidad graves, como erupción cutánea, dificultad respiratoria leve, hinchazón facial leve y eosinofilia (aumento del número de glóbulos blancos)2.
Adakveo vs Oxbryta: Comparación de precios
Cuando se trate de precios de medicamentos que aún no están aprobados o disponibles, debe tomarlos sólo como indicativos. El precio final puede variar en función de su ubicación o del proveedor.
Costes anuales Adakveo
La dosis recomendada de Adakveo es de 5 mg/kg de masa corporal cada 4 semanas. Esto significa 13 infusiones al año. Para una persona que pese 60 kg, serían necesarias 13 infusiones x 300 mg de Adakveo, es decir, 39 viales del medicamento.
A un precio de unos 5.214 euros por vial de 100 mg, el coste anual de un tratamiento Adakveo asciende a unos 203.346 5 euros.
Costes anuales de Oxbryta
La dosis recomendada de Oxbryta para pacientes con un peso corporal superior a 40 kg es de 1.500 mg de Oxbryta una vez al día, equivalente a 3 comprimidos de 500 mg cada uno.
Un envase de 90 comprimidos de 500 mg cuesta unos 40.365 EUR y es suficiente para un mes, según la dosis recomendada anteriormente. Por tanto, el coste anual del tratamiento con Oxbryta asciende a 484 380 EUR 6.
¿Dónde están autorizados Adakveo y Oxbryta ?
Adakveo crizanlizumab) está aprobado actualmente en varios países, entre ellos EE. UU., Canadá y Australia 7,9,10. Su autorización de comercialización condicional en la UE se revocó en mayo de 2023 3.
Oxbryta voxelotor) está autorizado en EE.UU., la UE y Canadá 4,8,9. Sin embargo, en la UE, Oxbryta aún no está ampliamente disponible en el mercado, ya que el tiempo transcurrido entre la autorización y el lanzamiento al mercado puede variar significativamente de un país a otro.
Adakveo u Oxbryta no están (ya) aprobados o disponibles en su país? Si usted y su médico opinan que estos tratamientos podrían beneficiarle, póngase en contacto con nuestro equipo de expertos en Acceso a Medicamentos. Podemos darle un presupuesto personalizado para conseguirle el medicamento.
Referencias:
- PUNTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN. Novartis, consultado el 27 de septiembre de 2023.
- PUNTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN. Oxbryta, Consultado el 27 de septiembre de 2023.
- Adakveo | Agencia Europea de Medicamentos. Agencia Europea de Medicamentos, consultado el 27 de septiembre de 2023.
- Oxbryta | Agencia Europea de Medicamentos. Agencia Europea de Medicamentos, consultado el 27 de septiembre de 2023.
- Comprar Adakveo (crizanlizumab) en línea. Everyone.org, Consultado el 27 de septiembre de 2023.
- Comprar Oxbryta (voxelotor) en línea. Everyone.org, Consultado el 27 de septiembre de 2023.
- Adakveo. Therapeutic Goods Administration (TGA), consultado el 27 de septiembre de 2023.
- La FDA aprueba un medicamento para tratar la anemia falciforme en pacientes pediátricos. FDA, 17 de diciembre de 2021.
- Nuevos medicamentos aprobados en 2019 - Meds Entry Watch. Canada.ca, 10 de febrero de 2021.
- La FDA aprueba la primera terapia dirigida para tratar a pacientes con una complicación dolorosa de la anemia falciforme. FDA, 15 de noviembre de 2019.